[이코노믹리뷰=곽예지 기자] 휴온스바이오파마가 '보톡스'로 대표되는 보툴리눔 톡신 의약품 시장에서 신흥 강자로 떠오르고 있다. 이 기업은 해당 의약품과 관련한 성과를 잇달아 도출하면서 바이오 사업의 전문성 및 경쟁력을 강화하고 있다.
휴온스바이오파마는 이달에만 보툴리눔 톡신 '리즈톡스'(수출명 휴톡스) 50단위의 허가를 획득하고, 액상 제형화 기술 특허도 취득했다. 앞서 지난 4월에는 미국 아쿠아빗홀딩스와 '휴톡스'에 대한 4,000억원 규모의 기술수출 계약을 통해 북미 진출에 본격적으로 나섰다.
휴온스바이오파마는 지난 4월 휴온스글로벌(084110)로부터 보툴리눔 톡신 사업 부문이 물적 분할돼 설립된 기업이다. 보툴리눔 톡신 임상 개발과 바이오 신약개발 사업 등을 담당하고 있다. 에스테틱 분야의 바이오 신약 개발에도 매진하고 있다. 사업 안정화 이후에는 기업공개(IPO) 추진도 계획하고 있다.
보툴리눔 톡신 50단위 허가 획득…8월 200단위 허가 예정
19일 제약바이오 업계에 따르면 휴온스바이오파마는 이달 식품의약품안전처로부터 보툴리눔 톡신 리즈톡스 50단위의 허가를 획득했다. 기존에 발매된 100단위에 50단위가 추가되면서 2개의 제조단위를 보유하게 됐다. 오는 8월에는 200단위 허가를 받을 수 있을 것으로 보인다.
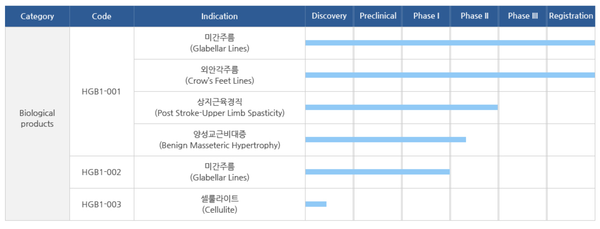
리즈톡스 50단위는 비교적 적은 양이 사용되는 미용 부문에서 사용된다. 허가 절차를 밟고 있는 200단위의 경우 임상시험 중인 뇌졸중 후 상지근육 경직 치료와 양성교근비대증 등 치료 영역에서 주로 사용될 것으로 보인다.
휴온스바이오파마 관계자는 “보툴리눔 톡신은 시술 부위 및 범위에 따라 투여 용량이 결정되기 때문에 의료진과 환자의 필요에 따라 적합한 용량을 선택해 사용한다”며 “의료 현장에서 선택의 폭을 넓히기 위해 신규 용량 허가를 추진했다”고 설명했다.
리즈톡스는 현재 미간주름, 눈가주름 개선 등 미용 영역 적응증을 보유하고 있다. 치료 영역에서는 뇌졸중 후 상지근육 경직 치료에 대한 임상 3상 시험계획(IND) 승인을 앞두고 있다. 적응증 획득은 2023년에 할 수 있을 것으로 전망된다. 양성교근비대증에 대한 임상 2상도 진행하고 있다.
보톨리눔 톡신 액상 제형화 기술 특허 취득…HU-045 임상 추진
휴온스바이오파마는 이달 분말 형태의 보툴리눔 톡신을 액상 제제로 만드는 기술 특허도 확보했다. 이는 보툴리눔 독소 안정화 액상 조성물에 대한 국내 특허다.
이번에 확보한 특허기술은 기존 분말 형태 보툴리눔 톡신 제제가 희석 과정을 거쳐야 했던 단점을 보완한 기술이다. 체온과 pH에 적합한 조건 하에 비동물성 제제를 활용해 보툴리눔 톡신 안정화 효과를 입증했다.
휴온스바이오파마 관계자는 “액상형 제제 특허 기술이 보툴리눔 톡신 외 바이오의약품 분야에서도 다방면으로 활용이 가능해 상업적 가치가 높을 것"이라며 “자체 개발 중인 내성 발현을 낮춘 신규 보툴리눔 톡신인 'HU-045'에 적용하는 것 외 다수의 기업과의 협업도 추진할 수 있을 것으로 보고 있다”고 말했다.
휴온스바이오파마는 보툴리눔 톡신 리즈톡스 미용영역 및 치료영역 적응증 확대에 속도를 내고 있다. 내성 발현을 줄인 신규 보툴리눔 톡신 HU-045의 임상도 추진 중이다. 지난해 12월 미간주름 개선에 대한 임상 1상을 종료했고, 다음 단계 임상을 준비하고 있다.
美에 휴톡스 4,000억원 기술수출…2024년 북미 시장 진출 목표
휴온스바이오파마는 지난 4월 미국 아쿠아빗홀딩스와 주름 개선 보툴리눔 톡신 제품인 ‘휴톡스’에 대한 4,000억원 규모의 기술수출 계약을 통해 북미 진출에 나섰다.
계약 규모는 로열티 및 마일스톤 등을 포함해 10년간 총 4,000억원 규모다. 현지 임상 및 허가, 마케팅, 영업은 아쿠아빗이 담당한다. 휴온스바이오파마는 국내에서 생산한 휴톡스 완제품을 공급한다.

휴톡스의 북미 시장 진출은 오는 2024년을 목표로 하고 있다. 연내 미국 식품의약국(FDA)에 임상시험을 신청해 오는 2023년까지 현지 임상 완료를 목표한다. 이후 모든 등록 절차를 완료하고 출시할 계획이다.
휴톡스는 현재 카자흐스탄, 이라크 및 볼리비아에서 허가를 받았다. 현재 중국을 비롯한 러시아, 유럽, 중남미, 브라질 등 해외 주요국 수출을 위한 임상 및 허가 절차가 진행 중이다. 중국에서는 임상 3상 진입 준비 중이며, 러시아에서는 품목허가를 앞두고 있다. 브라질, 페루 등 중남미 국가에 대한 현지 품목허가를 위한 등록 절차도 진행되고 있다.
휴온스바이오파마 관계자는 “FDA 허가를 획득한 휴온스그룹의 생산∙품질관리 등을 통해 휴톡스의 북미 시장 진출을 이뤄낼 것"이라고 말했다.


